Oganesson
Việc tạo ra các nguyên tố siêu nặng mới là một bài tập thực hành trong việc theo đuổi bóng ma nguyên tử. Những hạt nhân vô cùng không bền này được tạo ra với số lượng đếm bằng một chữ số, và thường chỉ tồn tại trong một phần hết sức nhỏ của một giây trước khi tự hủy mất. Bởi thế, các nhà nghiên cứu phải rây rê giần sàng mớ hỗn tạp đồng vị con cháu của chuỗi phân rã để cố tìm ra đường nét mờ mờ của cái bóng lởn vởn của chúng. Nguyên tố 118 đúng là nguyên tố ma tri. Phải tốn cỡ 10 tỉ tỉ va chạm của các hạt nhân calcium trên bia californium mới tạo ra được một nguyên tử với chu kì bán rã ước tính 0,89 mili giây. Kể từ 2005, chỉ có ba hoặc bốn nguyên tử Og-294 được tìm thấy. Đội hợp tác Dubna-Berkeley đã xuất tên gọi vinh danh Yuri Oganessian, một nhà khoa học hạt nhân người Nga.
Với việc bổ sung khí hiếm nặng nhất này, chu kì 7 đã đầy đủ. Thế nhưng đây có phải là nguyên tố cuối cùng của bảng tuần hoàn hay chưa?

Các khám phá tương lai
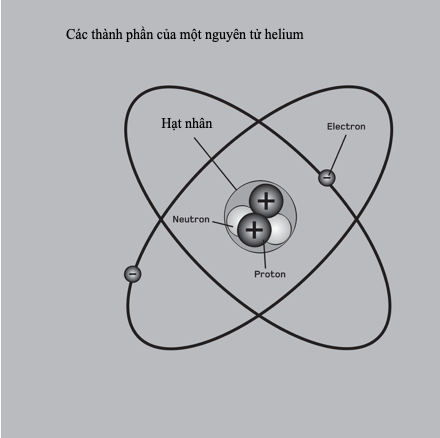
Mô hình lớp vỏ hạt nhân, được thiết lập vào cuối thập niên 1960, đề xuất rằng proton và neutron điền đầy các lớp vỏ trong hạt nhân nguyên tử theo kiểu giống như elecron tạo nên các lớp vỏ bên ngoài hạt nhân. Y hệt như các lớp vỏ electron điền đầy đem lại sự ổn định hóa học, các nguyên tố có ‘lớp vỏ hạt nhân’ điền đầy sẽ không còn bị phân rã phóng xạ. Cái gọi là các số ‘thần kì’ và ‘thần kì kép’ này của proton và neutron giải thích tại sao các đồng vị như helium-4, oxygen-16, calcium-48 và chì-208 có dồi dào trong vũ trụ.
Khi các nguyên tố vượt quá số nguyên tử 102 dễ dàng tổng hợp cũng dễ dàng phân hạch, Glenn T. Seaborg đề xuất rằng có một ‘biển bất ổn’, sau đó là một ‘đảo ổn định’ kéo từ nguyên tố 112 đến 118. Tuy nhiên, những hạt nhân này còn lâu mới ổn định, còn một công trình lí thuyết gần đây dự đoán một đảo ổn định xung quanh unbibium-306 (số nguyên tử 122). Câu hỏi vẫn còn bỏ ngỏ là: liệu có tìm được hay không các nguyên tố vượt quá 118? Dường như vẫn có khả năng cho một số hóa học khác lạ nào đó vượt ngoài địa hạt của bảng tuần hoàn hiện nay.
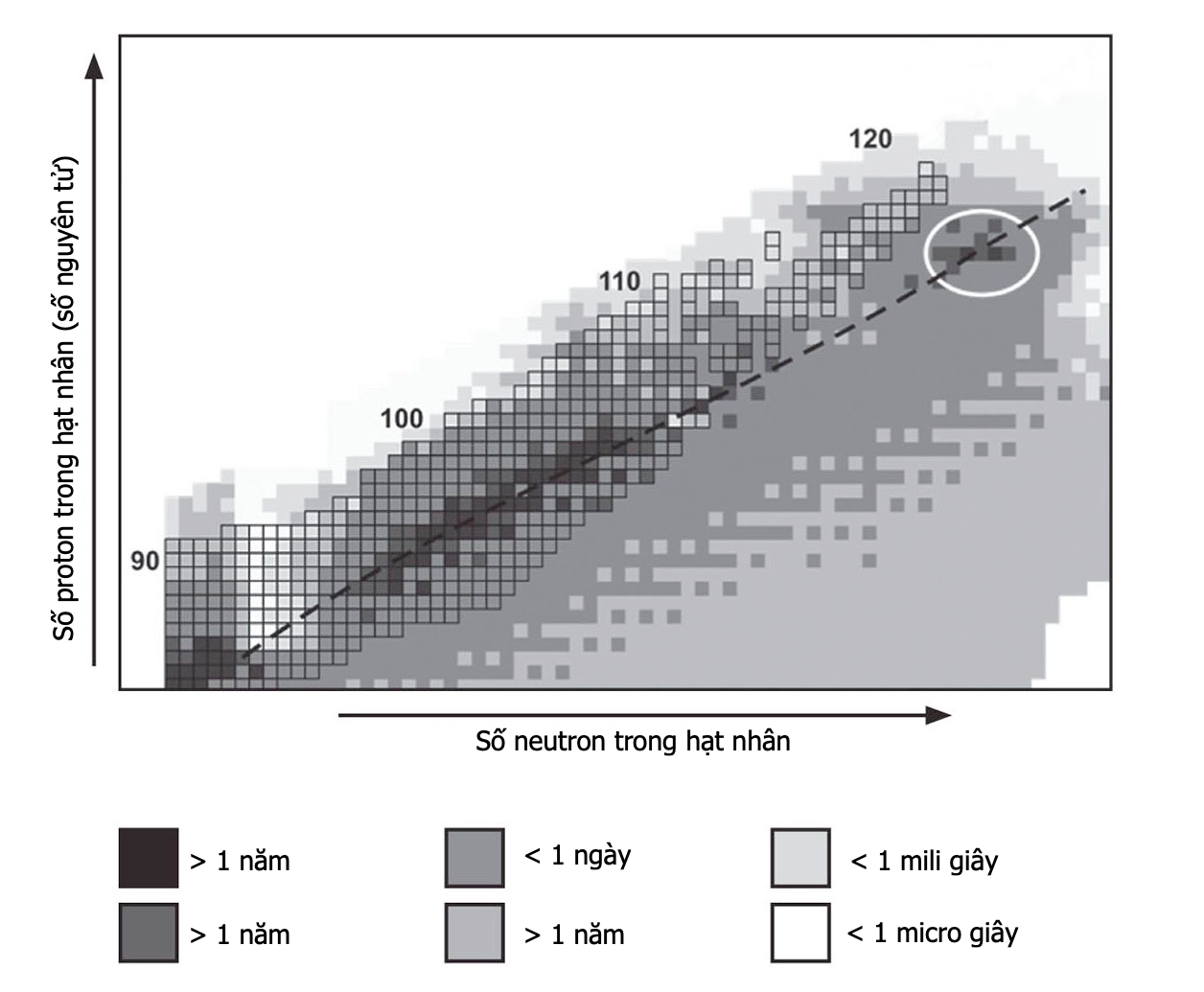
‘Bản đồ’ này của các đồng vị nặng sử dụng mã màu để nhận dạng các đồng vị có chu kì bán rã đã đo hay đã tính được. ‘Đảo ổn định’ như dự đoán được khoanh tròn.
CHÚ GIẢI THUẬT NGỮ
Acid
Dung dịch lỏng vị chua, phản ứng với base và kim loại bằng cách cho đi proton.
Base
Những chất vị đắng trung hòa acid, phản ứng với chúng tạo ra muối. Nói chung, base là chất nhận proton. Một base tan trong nước được gọi là kiềm.
Chu kì bán rã
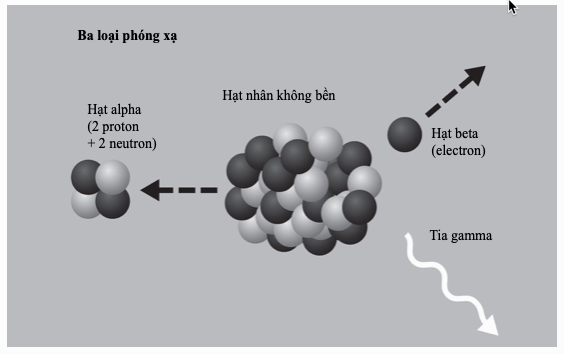
Thời gian cần thiết cho một nửa lượng chất của một đồng vị phóng xạ cho trước phân rã thành dạng khác thông qua sự phóng xạ.
Đất
Một tên gọi cổ xưa chỉ một chất hóa học bền. Các loại đất từng được xem là các nguyên tố, nhưng ngày nay người ta biết chúng là các hợp chất, thường là oxide.
Độ âm điện
Xu hướng của nguyên tử hút các electron liên kết với nó. Fluorine là nguyên tố hóa học có độ âm điện lớn nhất.
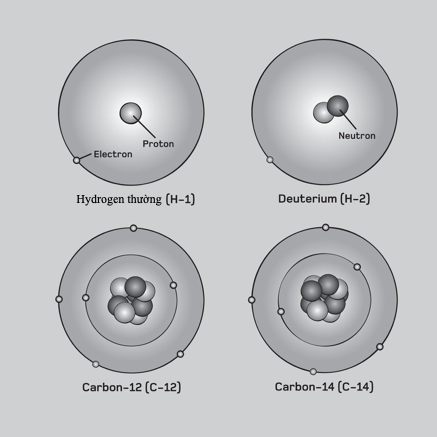
Đồng vị
Một nguyên tử thuộc một nguyên tố với một số lượng neutron nhất định. Các đồng vị của một nguyên tố cho trước đều có cùng số nguyên tử (số proton) nhưng có số khối (số proton + neutron) khác nhau.
Đồng vị phóng xạ
Một đồng vị có các hạt nhân không bền và dễ dàng phân hủy qua sự phóng xạ.
Electron hóa trị
Các electron trong orbital ngoài cùng của một nguyên tử; các electron có thể tham gia liên kết.
Hợp chất
Một chất hay một phân tử gồm các nguyên tử thuộc hai hoặc nhiều nguyên tố khác nhau.
Ion
Một nguyên tử hay một nhóm nguyên tử mang điện do sự mất cân bằng giữa số electron tích điện âm và số proton tích điện dương.
Khoáng chất
Một chất rắn vô cơ có mặt trong thiên nhiên với các nguyên tử sắp xếp đều đặn.
Mạng tinh thể
Tổ chức 3-D của các nguyên tử bên trong một tinh thể, được cấu tạo bởi những đơn vị lặp lại.
Muối
Một hợp chất ion hình thành khi acid phản ứng với base, kim loại hoặc ion phân tử, hoặc khi kim loại phản ứng với phi kim. Các muối bền thỉnh thoảng được gọi là ‘đất’.
Nguyên tố
Một chất có các nguyên tử có cùng số lượng proton trong hạt nhân của chúng, và do đó có hóa tính giống nhau.
Nguyên tử
Đơn vị cơ bản của nguyên tố hóa học. Nguyên tử được cấu tạo bởi những hạt hạ nguyên tử nhỏ hơn – proton và neutron trong hạt nhân ở trung tâm, và electron trong các orbital xung quanh hạt nhân.
Orbital electron
Còn gọi là orbital nguyên tử, orbital là các vùng bên trong một nguyên tử trong đó xác suất tìm thấy electron là lớn nhất. Trong một nguyên tử cho trước, có nhiều orbital và mỗi orbital gắn liền với một năng lượng nhất định. Trong các nguyên tử, electron không được tìm thấy bên ngoài các orbital.
Phân tử
Một nhóm gồm hai hoặc nhiều nguyên tử trung hòa điện liên kết hóa học với nhau.
Polymer
Một ‘phân tử vĩ mô’ cỡ lớn được cấu tạo bởi những đơn vị con lặp lại. Polymer có thể là phân tử thiên nhiên hoặc tổng hợp.
Số khối
Số lượng nucleon (proton và neutron) trong một hạt nhân nguyên tử. Số khối không bằng khối lượng đo được của một nguyên tử, hay trọng lượng nguyên tử của nó.
Số nguyên tử
Số lượng proton trong hạt nhân nguyên tử của một nguyên tố.
Số thần kì
Số lượng nucleon (proton hoặc neutron) điền đầy hoàn toàn một lớp vỏ bên trong hạt nhân nguyên tử. Các số thần kì được chấp nhận rộng rãi là 2, 8, 20, 28, 50, 82, và 126.
Thể vẩn
Hỗn hợp gồm hai pha – các hạt chất rắn lơ lửng trong một chất lỏng. Các thể vẩn cuối cùng sẽ lắng xuống do tác dụng của trọng lực.
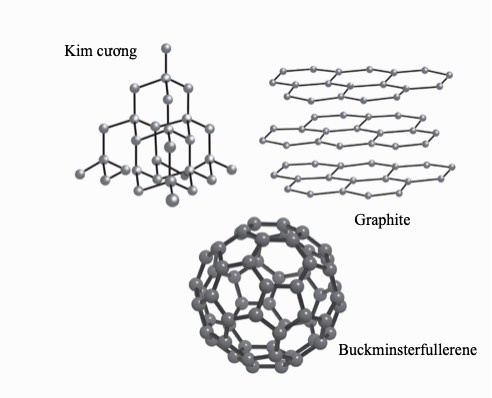
Thù hình
Tính chất của các nguyên tố hóa học nhất định có hai hoặc nhiều hình thức bền, ở cùng trạng thái vật lí.
Trạng thái oxy hóa
Một con số cho biết số lượng electron nhận vào, cho đi hay chia sẻ bởi một nguyên tử trong liên kết hóa học.
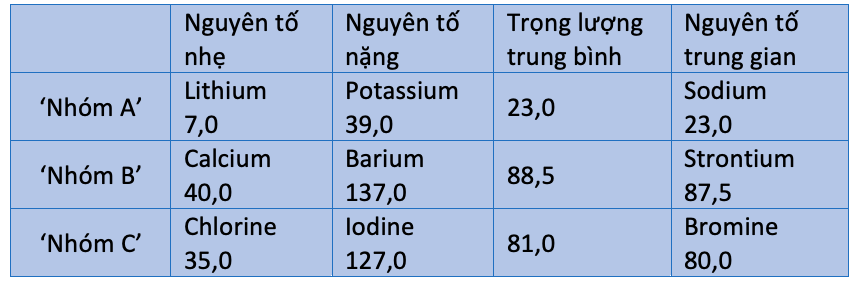
Trọng lượng nguyên tử
Còn gọi là khối lượng nguyên tử tương đối, đây là số đo về khối lượng nguyên tử trung bình của một nguyên tố. Nó được xây dựng bằng cách so sánh một nguyên tố với khối lượng trên lí thuyết của 1/12 một nguyên tử carbon. Giá trị trung bình này phụ thuộc vào hàm lượng của các đồng vị – số lượng neutron khác nhau làm sai lệch giá trị đó, vì thế hydrogen với số khối 1 có trọng lượng nguyên tử 1,008.
Bảng tuần hoàn hóa học tốc hành
Dan Green | Bản dịch của Thuvienvatly.com
<< Phần trước | Phần tiếp theo >>