Các kiểu hình trong bảng tuần hoàn
Ban đầu dùng hành trạng hóa học giống nhau làm nguyên lí tổ chức, bảng tuần hoàn đã làm bùng nổ các ‘họ hóa chất’ của các nguyên tố có liên quan. Các kim loại chiếm hơn 75 phần trăm các nguyên tố, chia làm kim loại kiềm, kiềm thổ, chuyển tiếp, lanthanoid, actinoid và – với các đặc trưng kim loại kém nhất – các kim loại hậu chuyển tiếp. Một dải mỏng á kim phân chia kim loại với phi kim, còn các khí trơ chạy thẳng xuống mạn cuối cùng bên phải của bảng tuần hoàn.
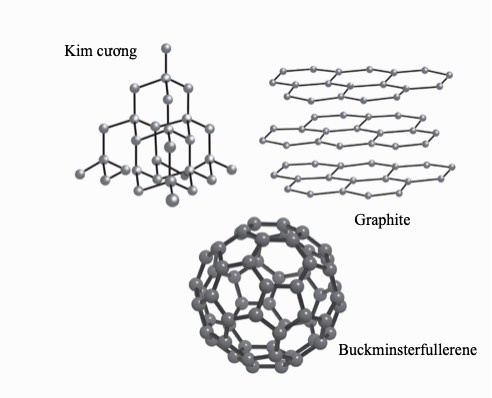
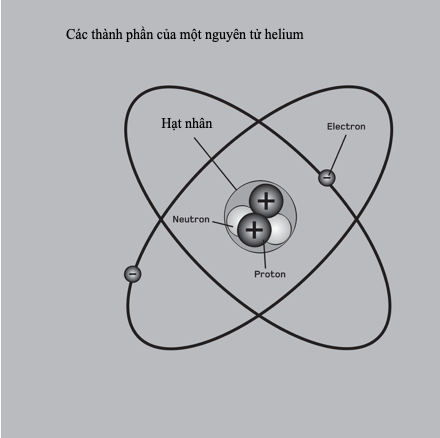
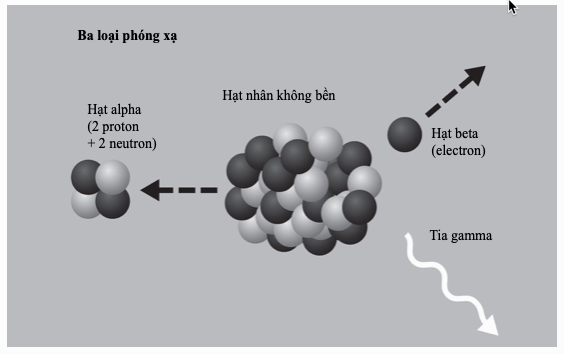
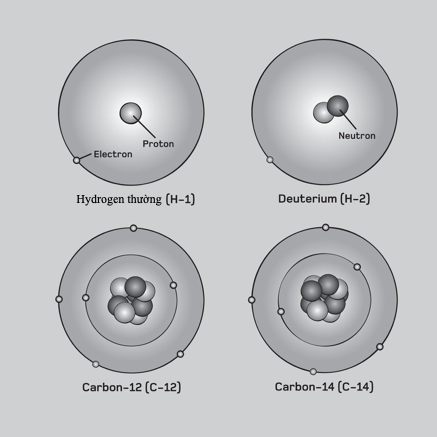
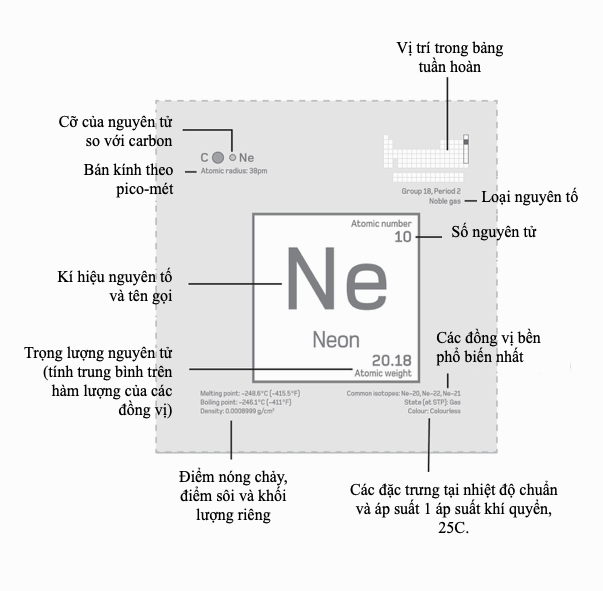
Không chỉ là một bảng tính đơn giản cho các nguyên tố, bảng tuần hoàn còn là một cấu trúc triết học, nó đủ kiên cố để tích hợp những khám phá sau này về số nguyên tử, cấu hình electron, và các đồng vị. Mỗi ô biểu diễn một tập hợp đồng vị, một kiểu ‘trung bình’ mà Dmitri Mendeleev gọi là ‘nguyên tố thật sự’. Bảng tuần hoàn là một tấm bản đồ về những viên gạch cấu trúc của vật chất, biểu lộ nhanh cấu tạo, hành trạng và xu hướng thay đổi các tính chất của một nguyên tố.
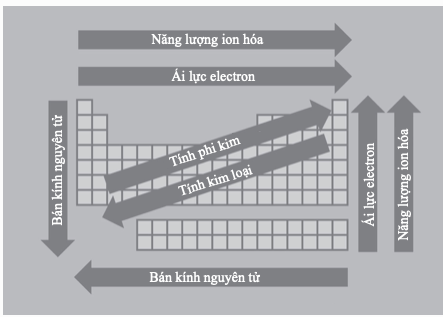
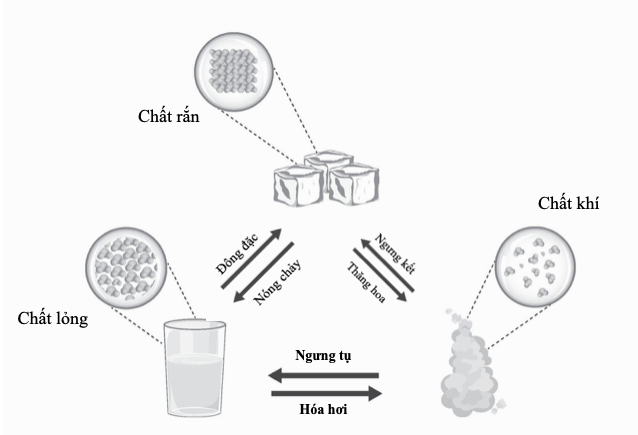
Sức mạnh của bảng tuần hoàn không chỉ ở cách nó sắp xếp 105 chất rắn, 11 chất khí và 2 chất lỏng, mà nó còn ở cách nó bộc lộ các liên hệ tiềm ẩn và các kiểu hình giữa các nguyên tố.
Nhóm và chu kì
Bảng tuần hoàn bố trí các nhóm theo cột dọc, và các chu kì theo hàng ngang. Học sinh ở trường phổ thông được dạy rằng các nguyên tố nhóm chính – các nhóm đứng đầu bởi lithium, beryllium, boron, carbon, nitrogen, oxyegn, fluorine và helium – được đánh số thứ tự nhóm từ 1 đến 8. Tuy nhiên, hệ thống này trở nên lộn xộn khi cần phải nói về 10 cột nguyên tố chuyển tiếp nằm giữa nhóm 2 và 3. IUPAC – Hiệp hội Quốc tế Hóa học và Hóa học Ứng dụng – chứng thực một danh pháp 1-18 để tránh rắc rối. Họ lanthanoid và actinoid rơi giữa nhóm 2 và 3. Các hàng của bảng tuần hoàn chạy từ chu kì 1, với chỉ 2 nguyên tố, qua đến chu kì 7, với 32 nguyên tố. Số nguyên tử tăng dọc theo chu kì, với số gia bằng một – tương đương với việc mỗi lần thêm một proton vào hạt nhân nguyên tử. Số lượng nguyên tử khác nhau trong mỗi chu kì tương ứng với số electron tối đa mà mỗi mức năng lượng liên tiếp chứa được. Các nguyên tố trong một nhóm có cấu hình electron lớp vỏ hóa trị y hệt nhau.
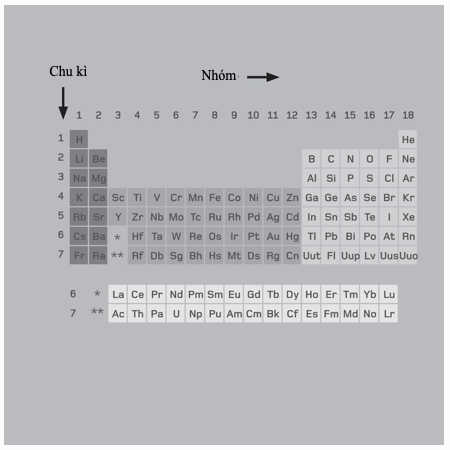
Bảng tuần hoàn hóa học tốc hành | Dan Green
Bản dịch của Thuvienvatly.com