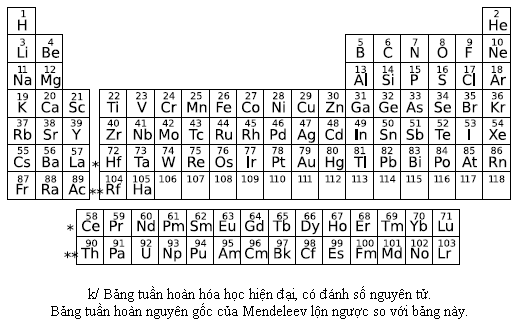
Số nguyên tử: 5
Trọng lượng nguyên tử: 10,8111
Màu: biến đổi
Pha: rắn
Phân loại: kim loại
Điểm nóng chảy: 2.076oC
Điểm sôi: 3.927oC
Cấu trúc tinh thể: hình hộp mặt thoi (giống boride)
Boron là một trong những anh hùng chưa được tôn vinh của bảng tuần hoàn hóa học. Nó thiếu sức quyến rũ của vàng hoặc bạch kim, và có tên gọi không ‘kêu’, nhưng nó có thể gây ra nhiều xảo thuật hóa học hấp dẫn, và các hợp chất của nó đã tỏ ra hữu ích trong hàng thế kỉ qua.
Boron là một thành phần chính trong borax, còn gọi là sodium borate, sodium tetraborate hay disodium tetraborate. Đây là một muối của acid boric, thường xuất hiện dưới dạng chất bột trắng và hòa tan dễ dàng trong nước. Nó được dùng làm chất tẩy rửa, thuốc diệt nấm và thuốc trừ sâu trong trong cả thiên niên kỉ, và còn dùng làm chất hãm lửa, một thành phần trong gốm sứ và dùng làm chất gây cháy để dễ bề xử lí hơn với kim loại nóng chảy.
Tên gọi boron có xuất xứ Arab boraq, nghĩa là “borax”. Muối này lần đầu tiên được tìm thấy ở Tây Tạng và được vận chuyển tây tiến qua Con đường Tơ Lụa (một lộ trình mậu dịch cổ thông thương giữa Trung Hoa và phương Tây) đến vùng Cận Đông và châu Âu. Borax còn được nhắc tới trong “Phần mở đầu” của tác phẩm Những chuyện kể vùng Canterbury của nhà thơ người Anh Geoffrey Chaucer, được viết vào cuối thế kỉ 14. Borax sau này được dùng làm mĩ phẩm và trộn chung với dầu, vỏ trứng nghiền mịn và các thành phần khác để tạo ra nét thơ ngây trắng mịn mà Nữ hoàng Anh Elizabeth I ưa chuộng.
Sự có mặt của boron lần đầu tiên được để ý đến vào năm 1732 dưới dạng một ngọn lửa màu lục khác lạ bởi nhà hóa học người Pháp Geoffroy. Có thể thu được ngọn lửa này bằng cách xử lí borax với acid sulfuric để biến boron thành acid boric. Sau đó thêm cồn vào và acid bốc cháy. Vào năm 1808, nhà hóa học người Anh Humphry Davy đã cố tách boron nguyên chất ra khỏi borate bằng cách nung nó với kim loại potassium. Ở Paris, Joseph Louis Gay-Lussac và Louis-Jacques Thénard đang theo đuổi quá trình y như vậy, nhưng cả hai người họ lẫn Humphry chẳng có ai tách được boron nguyên chất. Cho đến năm 1892 thì Ezekiel Weintraub thuộc Công ti Điện lực General Electric ở Mĩ mới đốt được một hỗn hợp gồm hơi boron chloride và hydrogen.
Boron chỉ được tìm thấy dưới dạng các khoáng chất borate trên Trái đất. Những bể trầm tích lớn của borate có ở Thung lũng Chết thuộc California, ở Mĩ, đồng thời ở vùng Tuscany thuộc Italy. Ngày nay, boron chỉ yếu được khai khoáng ở Mĩ, Thổ Nhĩ Kì, Tây Tạng và Chile.

Một mẩu boron kết tinh, nguyên chất. Bạn sẽ không tìm thấy cái gì như thế này trong thiên nhiên, vì trong thiên nhiên boron chỉ tồn tại ở dạng hợp chất với các nguyên tố khác – ví dụ như các khoáng chất kernite và colmanite.
Boron tồn tại ở một vài dạng thù hình khác nhau. Phổ biến nhất là boron vô định hình, một chất bột màu đen phản ứng với các kim loại tạo ra boride nhưng không phản ứng với oxygen, nước hoặc acid và các kim loại kiềm.
Điều thú vị là nếu boron kết hợp với nitrogen thì tinh thể được tạo ra (boron nitride) cứng ngang ngửa với kim cương. Tinh thể này rẻ tiền hơn nhiều và có nhiệt trở lớn hơn biến chúng thành chất mài mòn hữu ích trong ngành luyện thép. (Trong công nghiệp, các chất mài mòn được dùng để làm sạch, loại bỏ vật liệu thừa, mài sắc và cắt.)
Nếu bạn có một cục đồ chơi Silly PuttyTM (còn gọi là Thinking Putty) trên bàn làm việc, bạn có thể cảm thấy lí thú khi biết rằng chính boron liên kết polymer đã làm cho vật liệu nhiều màu sắc này vừa mềm và dễ dát mỏng khi cầm trong tay, và vừa cứng và đàn hồi khi bị vo cục. Hãy thử xem: nó có thể hữu ích khi xét đến tầm quan trọng của nguyên tố tiếp theo trong bảng tuần hoàn – đáng nói nhất là carbon.
















![[Ảnh] Kim tinh đi qua trước Mặt trời](/bai-viet/images/2012/06/sunvenus_sdo_1024.jpg)